肿瘤微环境与肿瘤的发生发展密切相关,越来越多的研究证实肿瘤微环境能够促进肿瘤细胞的增殖、诱导侵袭和转移、抑制抗肿瘤免疫,并降低抗肿瘤药物的疗效。因此,打破肿瘤微环境的保护壁垒已成为开发新抗肿瘤策略与药物的关键方向。徐翔晖教授团队以多肽药物与载体为基础,设计与发展了可高效干预肿瘤微环境的治疗策略与药物,成功调控了肿瘤微环境的细胞外基质及间质压(Small2023, 19, 202301656)、激活了肿瘤微环境的免疫原性(ACS Nano2023, 17, 17320)、解除了肿瘤微环境的免疫抑制(ACS Nano 2023, 17, 25638)等,从而有效遏制了肿瘤发展,显著提升了抗肿瘤疗效。相较于传统药物调控策略,多肽药物与载体虽然显著增强了肿瘤微环境调控的靶向性与疗效,但是仍面临难以持续且有效重塑肿瘤微环境的困境。
针对当前重编程肿瘤微环境策略在药效、时效与空间上的局限性,9001cc金沙以诚为本徐翔晖、李亚超团队提出了以设计与构建生物活性水凝胶重编程肿瘤微环境的新思路。生物活性水凝胶不仅能够模拟组织外基质的结构与功能,还能实现大范围且长效的肿瘤酸性微环境重塑,具备高效遏制肿瘤增殖、转移及侵袭的生物功能。研究发现,生物活性水凝胶可将实体瘤酸性微环境逆转至正常生理水平,降低肿瘤细胞酸性相关蛋白LAMP2的表达,下调TGF-β等转移相关蛋白表达,同步干预N-cadherin及E-cadherin的表达水平,遏制肿瘤上皮间质转化过程及肿瘤转移。深入研究表明,生物活性水凝胶还能够作为药物递送平台,促进小分子化疗药物和大分子蛋白药物发挥更大的抗肿瘤治疗功效。
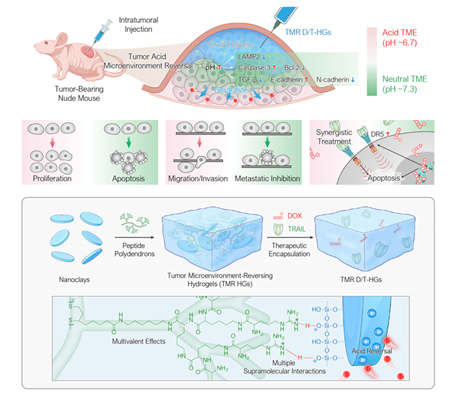
图 生物活性水凝胶重编程肿瘤酸性微环境与分子治疗增效
可重编程肿瘤酸性微环境的生物活性水凝胶研究成果为高效干预肿瘤发生发展提供了全新的策略,以“Inherent Tumor Microenvironment-Reversing Hydrogels: Potentiating Molecular Therapy Efficacy against Drug-Resistant Tumors”为题成功发表于Advanced Functional Materials。梁晓钰为第一作者(2023年硕士毕业生,已入职全球知名生物医药公司并从事相关研究),李亚超、徐翔晖为通讯作者。
